标准方案指南 中国儿童严重过敏反应诊断与治疗建议
- 健康养生
- 40秒前
- 6
作者:向莉1万伟琳2曲政海3赵京4周薇5徐保平6文利平2李丽莎2殷菊6姜楠楠1全美盈2申昆玲6
通信作者:申昆玲,Email:
作者单位:1国家儿童医学中心,首都医科大学附属北京儿童医院过敏反应科,国家呼吸系统疾病临床医学研究中心,北京;2中国医学科学院,北京协和医学院,北京协和医院儿科,北京 ;3青岛大学附属医院儿童医学中心,山东 青岛 ;4首都儿科研究所附属儿童医院哮喘防治中心与肺功能室,北京 ;5北京大学第三医院儿科 ;6国家儿童医学中心,首都医科大学附属北京儿童医院呼吸科,国家呼吸系统疾病临床医学研究中心,北京
本文刊发于 中华实用儿科临床杂志,2021,36(6):410-416.
引用本文:向莉,万伟琳,曲政海,等.中国儿童严重过敏反应诊断与治疗建议[J].中华实用儿科临床杂志,2021,36(6):410-416.DOI:10.3760/101-00157.
摘要和关键词
摘要儿童严重过敏反应发病率逐年升高,我国对儿童严重过敏反应尚存在认识和诊疗不足的问题。为进一步规范诊治儿童严重过敏反应,现基于国内外诊治实践参数及循证指南,对儿童严重过敏反应的发病机制、诱因和危险因素、临床表现及诊断、治疗和管理等方面进行了详细阐述,并提出了中国儿童严重过敏反应的诊断与治疗建议,旨在提高儿科医师对严重过敏反应的规范化管理水平,为未来制定中国儿童严重过敏反应诊疗指南奠定基础。
关键词严重过敏反应;食物过敏;儿童;肾上腺素
严重过敏反应()是一种主要由IgE介导的,临床表现为速发、危及生命、可累及全身多系统的超敏反应,多伴有皮肤黏膜系统表现,少数可仅表现为单一呼吸系统或心血管系统症状、体征,如严重的上气道梗阻、气道痉挛及低血压等,过敏性休克为危重症表现[1-2]。肌注肾上腺素为一线治疗。严重过敏反应的终身患病率为0.05%~2.00%[3]。约1/4的严重过敏反应发生在<18岁的儿童和青少年[4]。近年来儿童严重过敏反应的发病率呈上升趋势,尤其是低龄儿童[5-7]。近10余年来,国内外临床建立了严重过敏反应诊断标准、诊治实践参数和循证指南等[8-11],很大程度上提高了对严重过敏反应的认识,但在我国仍存在对儿童严重过敏反应治疗不足的问题[12]。为进一步规范诊治儿童严重过敏反应,我国儿科呼吸和过敏相关学术团体组织专家组广泛参阅相关文献,依据国内外相关防治指南及最新循证医学证据,制定了《中国儿童严重过敏反应诊断与治疗建议》,旨在提高儿科临床医师对中国儿童严重过敏反应的规范化管理水平,为未来制定中国儿童严重过敏反应诊疗指南奠定基础。1儿童严重过敏反应的发病机制严重过敏反应主要由IgE介导,肥大细胞、嗜碱性粒细胞、嗜酸性粒细胞(EOS)等释放生物活性介质引起的全身反应,分为致敏阶段和效应阶段,具有明显个体差异和遗传倾向。
致敏阶段:变应原诱导特异性IgE产生是严重过敏反应发生的先决条件。变应原进入机体后,激活特异性Th2细胞产生白细胞介素(IL)-4、IL-5等细胞因子,诱导特异性B淋巴细胞发生IgE类别转换并增殖、分化为浆细胞,浆细胞产生的亲细胞IgE抗体,在不结合抗原的情况下,通过其Fc段与肥大细胞和嗜碱性粒细胞表面高亲和力IgE Fc受体(FcεRⅠ)结合,使机体处于致敏状态。
效应阶段:处于致敏状态的机体再次接触相同变应原时,变应原与致敏肥大细胞或嗜碱性粒细胞表面IgE抗体特异性结合,使多个FcεRⅠ交联形成复合物,胞膜变构,活化信号启动,导致效应细胞活化并立即释放预先形成的组胺和类组胺介质,包括5-羟色胺、白三烯、类胰蛋白、血小板活化因子、肝素及花生四烯酸代谢产物,如前列腺素D2(PGD2)、白三烯B4(LTB4)、白三烯C4(LTC4)、白三烯E4(LTE4)等。组胺是引起严重过敏反应的重要介质,组胺释放后,作用于靶器官上的组胺受体(H1和H2受体),引起血管扩张、血管通透性增加、黏液分泌增多、支气管和胃肠道平滑肌痉挛,从而引起一系列临床症状。
效应细胞释放储存介质的同时,还产生EOS定向因子(IL-4、IL-5)、趋化因子CCL3和脂类介质。某些因子,如IL-4、IL-5等与EOS表面的相应受体结合,可刺激EOS表达FcεRⅠ并活化。EOS活化后,其胞质中嗜酸性颗粒脱出,释放一系列生物活性介质。其中一类是具有毒性作用的颗粒蛋白和酶类物质,主要包括EOS阳离子蛋白、主要碱性蛋白、EOS衍生的神经毒素和EOS过氧化物酶、EOS胶原酶等;另一类介质与肥大细胞和嗜碱性粒细胞释放的介质类似。共同加重过敏反应进程。
另外EOS还能释放组胺酶和芳基硫酸酯,抑制肥大细胞释放的组胺和白三烯(LTs),对炎性反应起到一定的抑制作用,因此EOS对严重过敏反应既有正向作用,亦有负向调节作用,因人而异。
严重过敏反应的临床表现并不完全一致,如迟发反应和双相反应。实验室检查发现,少数患者血清中特异性IgE(sIgE)含量极低,甚至检测不到,提示抑或与非IgE介导及多种过敏反应重叠发生有关[13]。有证据表明补体系统、C3a、C4a、C5a和中性粒细胞也参与严重过敏反应的发生[14]。值得临床研究。
双相反应原因较为复杂,除可能与过敏原延迟吸收[15]、血小板活化因子延迟释放及肥大细胞过度活化有关外[16]。EOS至关重要,一方面与EOS的毒性颗粒起效相对缓慢、半衰期较长,另一方面其对严重过敏反应的负调节机制可能被抑制有关。同时不除外2种以上类型的过敏反应交织等因素。
迟发反应可能与肥大细胞受体抗体或CD4+Th2细胞直接介导EOS的超敏反应有关。2儿童严重过敏反应的诱因和危险因素儿童严重过敏反应最常见的诱因为食物[17], 昆虫叮咬、药物诱因相对于成人较为少见[18-19]。由于膳食特征具有年龄依赖性,因此食物诱因具有年龄差异性,并且因饮食习惯和制备方式不同还存在地域差异。不同年龄段和在不同地区致敏食物分布具有如下特征。婴幼儿期在世界各地区最常见致敏食物均为牛奶、鸡蛋[20-23]。此外,在北美及欧洲国家,花生、坚果、贝类、鱼也是常见食物诱因[24],在亚洲,如日本、中国、韩国等国家,小麦和荞麦致敏则更为常见[22-23,25-26]。
有报道严重过敏反应在我国0~3岁儿童最常见的食物诱因为牛奶(62%),青少年最常见的诱因为小麦[26]。经口食入食物途径诱发严重过敏反应最常见,而非经口暴露食物变应原亦可诱发严重过敏反应,如通过吸入途径(吸入空气中的食物过敏原)[27]、皮肤接触(食物直接接触或化妆品中含有的食物变应原组分)[28]、肌内注射(疫苗中所含少量的鸡蛋成分)等[23,29]。除食物诱因外,昆虫叮咬、药物、疫苗也可诱发儿童严重过敏反应。
常见的儿童严重过敏反应危险因素包括:食物严重过敏反应病史、哮喘、花粉症、严重湿疹或特应性皮炎、荨麻疹、小麦过敏患儿在运动状态、过敏食物为花生/坚果等、有多重致敏状态等。特殊用药后增加严重过敏反应概率,如阿司匹林增加运动诱发严重过敏反应概率。婴幼儿危险因素包括:毛细支气管炎、反复发作喘息、先天性心脏病、湿疹、多重致敏状态等[30]。致死性严重过敏反应的危险因素包括哮喘、年龄>10岁、食物过敏类型为花生/坚果、延迟使用肾上腺素[31]。
严重过敏反应发生双相反应( )比率在儿童占0.4%~11.0%。即在首次症状完全缓解后1~72 h内无诱发因素触发情况下再次出现严重过敏反应的症状[32]。双相反应的危险因素包括:重度反应、皮肤黏膜受累、药物诱发(<18岁)、未知诱因、脉压差大、1次以上的肾上腺素治疗、严重过敏反应发生后应用糖皮质激素(<18岁)、延迟应用肾上腺素[32]。
儿童罕见迟发严重过敏反应,即在接触过敏原后数小时至数天内发作。3儿童严重过敏反应的临床表现及诊断3.1临床表现[33]严重过敏反应是一组综合征,可累及皮肤黏膜、呼吸和/或循环、消化等多个系统,表现为皮疹、水肿、喉鸣、喘息或低血压、剧烈呕吐等症状。
皮肤及黏膜症状和体征(发生率达90%)可表现为泛发性荨麻疹、瘙痒、潮红、唇-舌-悬雍垂肿胀、眶周水肿或结膜肿胀等;皮疹可出现在没有直接接触的部位。
呼吸系统症状和体征(发生率约为70%)可表现为流涕、鼻塞、喉鸣、失声、吞咽困难伴有流涎;喉水肿可导致气道阻塞,在短时间内出现危及生命的缺氧。支气管阻塞是危及生命的首要原因,特别是有哮喘的患者更易出现。可表现咳嗽、喘息、呼吸急促、双肺哮鸣音等。
胃肠道症状和体征(发生率约为45%)可表现为恶心、剧烈呕吐、腹泻和痉挛性腹痛。
心血管系统症状和体征(发生率约为45%)可表现为虚脱、晕厥、心率失常和低血压。
3.2婴幼儿严重过敏反应的临床表现婴幼儿严重过敏反应也可能出现如咳嗽、气喘、喘鸣、嗜睡、心动过速、循环衰竭和/或持续的胃肠道反应等在较大儿童出现的症状。最常累及的是皮肤黏膜系统(98%),如全身风团样皮疹、皮肤潮红、血管神经性水肿等;呼吸系统症状(59%),如咳嗽、喘息、喉鸣等;胃肠道症状(56%),如腹痛、持续性呕吐等;心血管系统的症状不常见,如低血压和心动过速等[34]。在某些情况下,持续性呕吐可能是唯一表现。非特异性的中枢神经系统症状,如停止玩耍、过度依赖成人陪伴、持续哭闹及嗜睡是亦常见的婴幼儿严重过敏反应的早期表现[33]。心源性休克在婴幼儿并不常见,通常为晚期表现[33]。
3.3临床诊断标准[1,11,35]儿童严重过敏反应诊断的主要依据为详细的发作史,包括症状和体征以及症状体征突然出现之前数分钟至数小时内所有暴露的已知或可疑变应原、可疑环境相关的详细信息。儿童的诊断标准和分级标准相似于成人,见表1。

如果符合下述2种情况中的1种,则极有可能诊断为严重过敏反应:(1)典型的皮肤表现合并至少1个其他系统的表现(呼吸系统、心血管系统、胃肠道系统);(2)暴露于已知或可疑变应原,导致呼吸和/或心血管系统症状,可无典型皮肤黏膜症状。
3.4早期识别儿童严重过敏反应的早期识别非常重要,特别是有过敏体质或过敏性疾病史者。暴露于已知或可疑变应原后数分钟至数小时内,出现皮肤瘙痒、皮肤潮红、荨麻疹、口唇或眼睑肿胀、胸闷、喘鸣、腹痛、腹泻、呕吐等症状,往往提示发生了过敏反应。部分患儿可能无皮肤黏膜症状,直接导致呼吸困难、喘息、低氧血症和血压下降、循环衰竭等症状,尤其是通过注射途径暴露者[36]。因此任何医疗机构对有发生过敏可能的任何医疗措施,均应给予观察监护。
婴幼儿的严重过敏反应早期诊断具有一定特殊性和挑战性。由于无法语言描述瘙痒、喉部发紧、胸闷等主观症状。照顾者应仔细观察婴儿的行为异常,如停止玩耍、依恋照顾者、困倦和持续哭闹是常见的早期症状[37]。心血管衰竭在婴儿中很少见,是典型的晚期症状。
3.5鉴别诊断[17,30]儿童严重过敏反应主要应与哮喘发作、晕厥和焦虑/惊恐发作相鉴别。急性哮喘发作有时不易与严重过敏反应鉴别,因喘息、咳嗽、气促均可发生于哮喘和严重过敏反应,但皮肤瘙痒、荨麻疹、血管神经性水肿、腹痛和低血压在急性哮喘很少见。晕厥可与严重过敏反应相混淆,但晕厥通常伴有苍白、大汗,而不伴有荨麻疹和消化系统症状。此外,异物吸入、精神心理疾病,如过度通气综合征、癫痫发作,内分泌疾病,如低血糖等需要与严重过敏反应相鉴别,见表2。婴儿严重过敏反应鉴别诊断与年长儿略有不同,如婴幼儿病毒感染后常出现荨麻疹样皮疹、呼吸道症状(如咳嗽、气促),虽出现2个系统症状,但不应诊断为严重过敏反应;婴幼儿期呕吐和腹痛也是多因素的,可能由多种非过敏病因导致 (如胃肠道感染性疾病、肠套叠等)。心动过速是婴幼儿严重过敏反应的早期表现,但也可继发于哭闹、发热和不适等原因,需要临床鉴别。

3.6临床分级标准[38-39]儿童严重过敏反应的分级标准见表3。
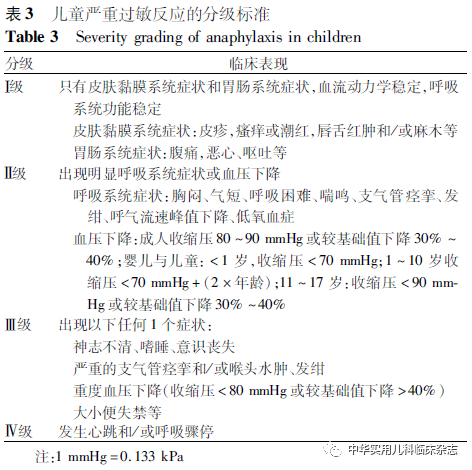
3.7双相过敏反应高危患儿建议延长观察时间至24 h。应教育所有患者发生双相反应的可能性以及避免已知的触发因素,早期识别过敏症状,注射肾上腺素治疗严重过敏反应,及时就诊变态反应专科医师。4严重过敏反应的治疗4.1治疗原则尽早使用肾上腺素肌注急救治疗,同时将患儿送往附近的急诊。抗组胺药和糖皮质激素仅为辅助药物,不能单独使用来治疗严重过敏反应,更不能替代肾上腺素。
4.2急救方案与具体药物剂量
4.2.1一线用药肾上腺素是严重过敏反应的首选急救药物,注射剂量根据患儿体质量计算, 1∶1 000肾上腺素0.01 mg/kg或按体质量7.5~25.0 kg:0.15 mg,体质量≥25.0 kg:0.30 mg[34],在严重过敏反应时使用肾上腺素没有绝对禁忌[8,33]。快速及时注射肾上腺素能降低患儿住院及死亡的风险[34,40-42](表4)。首选用药途径为大腿外侧肌注,不推荐皮下注射,因在发生严重过敏反应时,皮下组织血循环量不足,不利于药物吸收[43]。有研究表明,儿童患者肌注肾上腺素较皮下注射达到的血药峰浓度更高,且起效更快[44-45]。
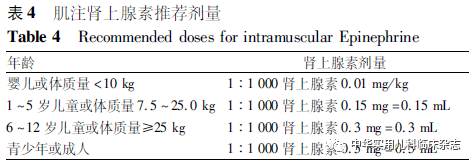
如果注射1次效果不佳,5~15 min后可重复注射,最多注射3次[43]。根据文献报道,有6%~19%的患儿需要注射第2次肾上腺素[46-48]。
肾上腺素可能带来短期不良反应:皮肤苍白、震颤、心悸、焦虑、头痛和头晕,多能自行缓解[49]。需注意不要把将肾上腺素的不良反应误诊为严重过敏反应症状再发。
4.2.2二线用药
4.2.2.1抗组胺药抗组胺药是治疗严重过敏反应的辅助药物,起效较慢,口服药30 min后开始起效[50],但血药浓度通常要60~120 min后才能达峰,还要再过60~90 min药物才能渗入血管外组织,从而发挥最大作用[10,51] ,因此,不能起到紧急挽救生命的作用,并非严重过敏反应的首选药物[10]。此外,抗组胺药的主要功能为抑制组胺受体活性,阻断组胺引发的过敏效应,但不能直接阻止肥大细胞脱颗粒,因此可用于缓解瘙痒、荨麻疹、水肿,但无法治疗低血压或气道阻塞症状,更不能替代肾上腺素[52] 。组胺H2受体拮抗剂治疗严重过敏反应的循证医学证据不足,不推荐在严重过敏反应中常规使用[53]。
4.2.2.2糖皮质激素全身糖皮质激素主要用于严重过敏反应的辅助治疗。因起效缓慢,起不到急救作用[32]。有研究表明,应用全身糖皮质激素的患儿住院时间更短[54],但并无足够证据支持糖皮质激素对双相严重过敏反应有预防作用[32]。
4.2.3其他治疗脱离诱发因素:在使用肾上腺素急救的同时,让患儿不再接触引起严重过敏反应的诱因。如果为静脉输注药物导致,则立即停止输液;如果为昆虫蜇刺后出现过敏,则立即远离昆虫聚集处;如果为食物过敏者,禁止催吐或洗胃,因为不能减轻过敏反应,有误吸的风险,可能会延误治疗。
4.2.4急救治疗[10,33,43]评估循环、气道、呼吸、皮肤症状等;快速启动急救流程、呼救。
体位:严重过敏反应伴有循环功能障碍,仰卧位、抬高下肢;呼吸窘迫者端坐位;昏迷意识不清者,侧卧位。
吸氧:高流量面罩吸氧。
循环功能障碍:建立静脉通道,晶体液扩容10~20 mL/kg,10~20 min内输入。必要时静脉滴注肾上腺素、多巴胺等升压药物。在静脉通路建立困难时,也可考虑予以骨髓内给药。
呼吸困难,有气道阻塞、喘息者予以吸入短效β受体激动剂,如沙丁胺醇,每15 min可重复吸入1次。如支气管舒张剂效果不佳,气道阻塞严重者,可建立人工气道及机械通气治疗。
4.2.5双相反应如有发生双相反应高危因素的患儿,应延长留观时间,建议留观至少6 h以上[32]。当发生双相反应时,治疗措施与初次发作时相似,首选药物仍为肌内注射肾上腺素0.01 mg/kg,或按体质量7.5~25.0 kg:0.15 mg,体质量≥25 kg:0.30 mg。5长期管理与教育5.1长期管理[55-57](1)经详细采集病史及变应原检查以明确可能的诱因。(2)根据目前指南处方肾上腺素并教会监护人/家长如何准确使用。(3)通过制定个性化书面文件向监护人告知急诊处置方案。(4)避免可能诱因防止再次发作。(5)定期随访评估过敏和耐受状态。
5.2预防措施与患者教育确诊导致严重过敏反应的诱因后,医师应告知患儿及其监护人如何避免患儿过敏的食物、药物或昆虫蜇刺。
5.2.1食物一旦确定过敏病因,医师需嘱咐患儿严格忌口。(1)避食过敏的食材和容易交叉过敏的食材(如牛奶过敏的患儿也不要食用羊奶)以及用这些食材制作的各种加工食品。(2)患儿监护人或大龄患儿本身应当养成进食前查看食品包装上配料表的习惯。(3)患儿避免接受他人分享的食品[58-59]。尽量在家中吃饭,减少外出就餐,外出就餐时也提前告知餐厅患儿需忌口的食材。(4)对于上幼儿园或上学的患儿,家长应明确告知教育机构患儿过敏的食物,以最大程度地降低意外误食过敏食材的风险[10,33,60]。(5)婴幼儿的食物过敏多数可随其年龄增长而自愈,所以应当每6~12个月在变态反应专科复诊,复查皮肤试验、血清特异性IgE检查及口服食物激发试验,若评估提示患儿已经产生耐受,则可恢复进食既往过敏的食物,有助于提高患儿生活质量,保证营养均衡[55]。
5.2.2药物医师应当在病历中明确记载患儿的药物过敏史;患儿应当严格避免使用曾引起严重过敏反应的药物,也应避免使用有交叉过敏的药物,可选择结构不同的另一类药物替代。如果因病情需要必须使用曾引起严重过敏反应的药物,可采用药物脱敏治疗[43]。
5.2.3昆虫蜇刺昆虫蜇刺曾引起严重过敏反应的患儿,应减少去野外活动;同时避免在户外吃饭、使用香水或穿色彩鲜艳的服装,以降低再次被蜇的风险。6结语严重过敏反应目前在国内尚未被充分认识,缺乏中国的流行病学数据,缺少高质量临床和基础研究论文发表,且中国人群严重过敏反应的诱因尚未充分阐明,肾上腺素作为一线治疗也仍未在临床实践广泛应用;同时也存在对严重过敏反应诊断和治疗的不足,这有可能造成治疗延误,增加重症结局风险。本“建议”旨在强调儿童严重过敏反应的及时、正确诊断;尽早明确诱因、降低再发风险;强调肾上腺素为治疗基石,对患儿进行长程管理、定期随访评估和制定个体化的急诊治疗方案;训练看护者/家长识别早期症状及使用肾上腺素。总之对于严重过敏反应,需进一步基于国际前沿进展,在国内开展相关研究,通过一段时间对“建议”的临床实践,以制定出适合中国儿童的诊疗方案。
参考文献略
(制作:新乡医学院期刊社网络与数字出版部)
上一篇
马玉成