2023CSCO指南会|结直肠癌-外科治疗部分(超全面)
- 健康养生
- 1小时前
- 177

一、基于 MMR/MSI 状态制定 M0 结直肠癌术前新辅助治疗策略:所有早期非转移性(M0)结直肠癌的新辅助治疗,都基于微卫星不稳定的策略来开展。
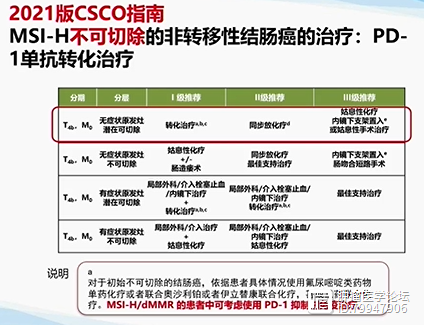
2021版CSCO最新指南,针对局部晚期、不可切除的T4b的结肠癌,推荐使用新辅助免疫治疗,基于 177和的标准化化疗,MSI-H疗效不佳。因此外科医生认为,不可切除的T4b高度微卫星不稳定的局部晚期结肠癌,应该考虑进行新辅助免疫治疗。

NCCN指南在2019年就提出了T4b结肠癌患者应该做新辅助化疗,2022版才提出做新辅助免疫,比我们晚推荐了一年。
1. MSI-H 结肠癌,新辅助 IO 正式写进推荐表格:

2023 CSCO指南把推荐细化为Ⅱ级推荐,如果是T4b局部晚期结肠癌会优先检测高度微卫星不稳定状态,采取新辅助免疫治疗。NICHE-2是针对此类患者的最突出的研究。NICHE-2研究在2018年的欧洲临床肿瘤学会(ESMO)会议上首次探索了微卫星高度不稳定肠癌的术前新辅助免疫治疗。去年在ESMO会议上公布了NICHE-2研究结果,研究对象全都是分期非常晚的高危Ⅲ期结肠癌患者,比如T4b和N2,也就是外科认为可切除的局部进展期患者,且全部为微卫星高度不稳定的患者。他们都接受了2个周期的PD-1纳武利尤单抗,以及1个周期的伊匹木单抗的新辅助免疫治疗,并在没有进行任何影像学评估的情况下进行手术。 这项研究主要终点是希望95%的患者能够安全地完成计划内的外科手术,不会因为新辅助免疫治疗而受到干扰。这是史上第一次以3年PFS为主要生存终点,希望将PFS从80%提高到93%,获益11%。结果证明这种治疗方案非常安全,即使使用双重免疫治疗,也只有2%的患者可能会干扰手术计划。从次要终点来看,有67%的患者达到了pCR,而95%的患者达到了MPR,也就是在显微镜下肿瘤细胞残留不超过5%。因此,提示未来可能是以免疫治疗为主的综合治疗,而不再是以外科为主。特别是对于没有发生远处转移微卫星高度不稳定的结肠癌患者。
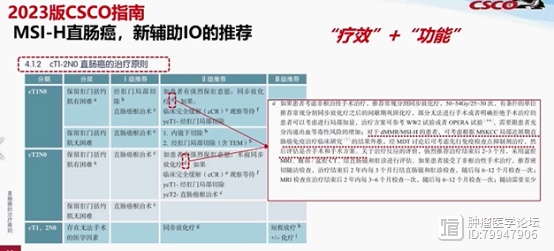
今年CSCO指南在直肠癌中的推荐考虑到了疗效和功能的平衡。即使是非常早期的T1、T2病例,如果传统外科手术可能影响患者功能,也应该首先检测微卫星高度不稳定的状态。因为对于微卫星高度不稳定的病人,单纯的免疫治疗就能完全治愈疾病,而无需传统的放疗、化疗和手术。
2.进展期结直肠癌以 MMR/MS 状态进行分层,增加注释:对于 dMMR 患者,可考虑新辅助免疫治疗;对于 pMMR LARC 增加多个小样本研究显示联合 IO 可提高 pCR 的注释。

局部进展期的直肠癌,根据微卫星不稳定的状态将疾病分为pMMR、MSS和dMMR三种类型。对于dMMR病例,应直接推荐术前新辅助免疫治疗,以优先考虑功能和疗效。尽管有许多小规模Ⅱ期临床研究支持,在pMMR患者中是否联合免疫进行术前新辅助治疗仍存在争议。术前新辅助化疗加免疫有可能提高治疗效果,但是需要慎重推荐。需参考临床研究或以多学科讨论和案例讨论来制定治疗方案。要重点关注新辅助免疫治疗在直肠癌中的应用情况。

2022年ASCO和NEJM同步发表的重要临床研究,入组了18例微卫星高度不稳定性进展期直肠癌患者,单独应用PD-1单抗治疗9个周期,14个病例全部达到cCR,因此提出了可以进行watch&wait",不需要化疗、放疗或手术治疗。研究入组了17例dMMR的直肠癌患者,使用信迪利单抗单药新辅助免疫治疗,患者中cCR和pCR的总体达到了75%。
3.MSI-H 早期直肠癌 II 级推荐有保肛意愿增加 IO 推荐的注释:这是一个非常经典的案例。入组的第8位病人是一位26岁的女研究生,刚毕业就发现患有局部进展期的直肠癌,距离肛门只有10公分,当时医生告诉她如果做手术就难以保住肛门,而做放化疗则会影响她的卵巢、子宫和生育功能,是典型林奇综合征。经过MSI-H筛查后,她被纳入临床研究中。经过4个周期的治疗后,达到了完全缓解(cCR)。完成8个周期的治疗后一直处于观察中。迄今为止,她的肿瘤已经完全消失。因此,无论是早期结肠癌还是直肠癌,新辅助治疗策略未来都应做出重大调整,即基于微卫星不稳定的状态进行治疗。哪些患者需要进行新辅助治疗,因人而异的,下面是一些策略。

NCCN 2023年版的结直肠癌指南将根据微卫星不稳定的状态开始治疗。
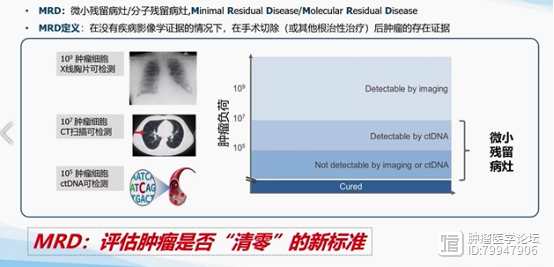
ctDNA可以用来检测微小残留病灶,未来会用于评估治疗后的肿瘤是否已被完全清除。目前除了血液系统肿瘤,ctDNA检测在所有的实体瘤中都得到了广泛的应用,而结肠癌更常见。

2022年版CSCO指南就已经提出了ctDNA检测MRD。由于目前资料还不是很完善,我们需要更多的证据来支持这个技术在实践中的应用。
二、ctDNA 检测 MRD 在结肠癌术后辅助化疗决策的价值:
1.病理学诊断原则增加注释 「s」,描述 ctDNA 检测 MRD 的价值,重点介绍技术方法优缺点:

更新的病理学指南提示,当前检测MRD非常需要技术。在检测tumor 的技术方案中,有两种主要方法:一是tumor-,即先从原发肿瘤组织中进行检测,然后再制定定制化的panel;另一个是tumor-naive。这两种方法的优劣尚未明确,未来需要更多的临床研究来加以确定。但个人认为,越来越多的数据支持tumor-的这种ctDNA MRD检测方法,这可能是肠癌MRD未来发展的主要方向之一。
2.术后辅助治疗增加注释 「i」 关于 研究 MRD 结果的描述:

今年的CSCO指南也提出了在制定Ⅱ期结肠癌化疗决策时需要参考MRD检测结果。主要证据来自于去年澳大利亚的 II研究。该研究入选的Ⅱ期结肠癌患者:1/3按照临床惯例进行治疗,2/3进行MRD检测,阳性的进行治疗,阴性的则不治疗。
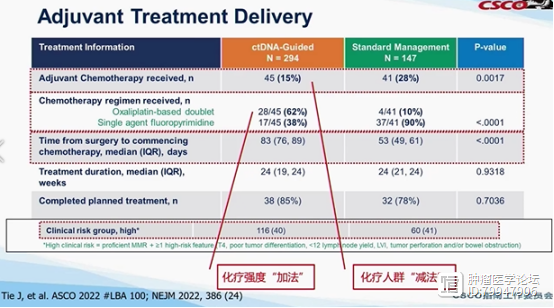
这项研究演示了MRD检测的加法和减法。通过MRD检测,需要化疗的人数从28%减少到15%,这是“减法”。同时,在化疗方案中进行了“加法”,MRD阳性的患者中,有90%使用奥沙利铂方案,而MRD阴性的患者中只有10%使用奥沙利铂方案。最终的结果是,两组患者的生存率完全相同。因此,从社会和国家的角度来看,基于MRD的更加精准的治疗是完全可行的。

MRD仍然存在很多技术问题,但可以指引一部分个性化的辅助治疗决策。临床医生应该甄别未来是使用ctDNA突变技术还是甲基化的技术。在ctDNA突变技术方面,需要考虑使用tumor-还是tumor-naive的方法。未来应该持续关注并开展更加前瞻性的临床研究。总的来说,今年的指南更新不多,但有一点非常重要一定要根据微卫星不稳定状态开展新辅助治疗。建议将这些信息传达给同行,促进更加精准的治疗决策。
刘云鹏教授、张艳桥教授,盛玮琪教授和王峰教授点评:1.指南的目的是为了提高规范性而不是提高探索性。指南中的影像评估和肠癌术前的同步放化疗非常值得关注,这两个方面是国家的弱项,急需通过指南进一步加强。在基层医院中,没有肿瘤专科影像医生,影像评估是一个比较大的挑战,肿瘤影像学相对于普通影像学的难度更大。希望通过指南,能够不断地提高基层医院的规范性。2.影像学的专科和精细化对肠癌的诊疗模式的贡献非常大.3.内科一直在讨论MSI-H,几乎没有MSS肠癌,期待大家在MSS型肠癌基础研究领域或临床研究领域去做贡献,这些才是真正能改变肠癌未来5年生存率的关键。4.ctDNA等新型的病理分子检测技术,离不开更多的能在实践中运用的临床研究数据的支撑。同时也需要病理实验室,通过努力更快的让这些检测方法在临床上标准化,获得结果一次性评价,真正在临床决策中体现其价值。所以在真正的临床实践中,提醒各位临床专家,在运用这些检测和使用这些数据时,一定要使用经过认证的平台,同时要做到质控,保证数据真实性,从而用于临床实践。5.对于dMMR,MSI-H肠癌的局限期或早中期的治疗,存在一定难度的。新辅助已经有很多证据了,但是现在越来越多的患者是在手术之后来咨询,比较缺乏辅助治疗的证据。在临床上会遇到到各种各样的病例,建议CSCO可以牵头做更多MSI-H辅助治疗的临床研究。对于精准治疗,因为95%的晚期患者都是pMMR的状态,这部分的患者是否可以有新的方案将免疫的冷肿瘤转化为热肿瘤,我们中心最近也即将启动一项相关的Ⅲ期临床研究,MRD检测的局限是瘤种依赖性,结直肠癌的证据非常多,但其他瘤种目前还没有太多的证据,在胃癌里MRD就不是特别有预测效能的检测方式,在未来也应做相关的探索。
采编:周天苗
欢迎点赞、在看、**
下一篇
携号转网剩余的话费处理








